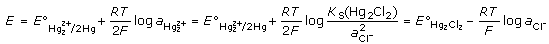| |||||
|
Referentní elektrodou rozumíme poločlánek s konstantním potenciálem, k němuž se vztahuje potenciál měrné (indikační) elektrody. Primární referentní elektrodou je standardní vodíková elektroda (SHE), jejíž potenciál je nulový při všech teplotách (definitoricky). V praxi se používají tzv. sekundární referentní elektrody, které jsou konstrukčně mnohem jednodušší než SHE. Jsou to elektrody II. druhu realizované jako kov pokrytý vrstvičkou své málo rozpustné soli ponořený do roztoku aniontů této soli. Nejpoužívanější jsou: kalomelová elektroda (rtuť pokrytá vrstvou Hg2Cl2 v roztoku KCl): Hg, Hg2Cl2 | KCl Na fázovém rozhraní se ustavuje rovnováha Hg2Cl2 + 2e Potenciál elektrody je určen aktivitou chloridových iontů v roztoku:
při 25 °C: E =Eo (Hg2Cl2) - 0,059 log a(Cl-) = 0,268 - 0,059 log a(Cl-) argentchloridová elektroda (stříbrný drátek pokrytý vrstvou Ag/AgCl v roztoku KCl) Ag, AgCl | KCl
AgCl + e
E =Eo (AgCl) - 0,059 log a(Cl-) = 0,222 - 0,059 log a(Cl-)
 Ag + Cl- Ag + Cl-merkurosulfátová elektroda (rtuť pokrytá vrstvou Hg2SO4 v roztoku K2SO4 nebo H2SO4): Hg, Hg2SO4 | K2SO4
Hg2SO4 + 2e
E =Eo (Hg2SO4) - 0,029 log a(SO42-) = 0,615 - 0,029 log a(SO42-)
 2Hg + SO42- 2Hg + SO42-
| ||||||||||||||||||||||||