|
- Příklad 3.63
- Směs KCl a KBr hmotnosti 0,200 g byla rozpuštěna a stanovena
argentometricky. Spotřeba 0,0996M-AgNO3 byla 18,20 ml. Jaký je hmotnostní obsah
jednotlivých složek ve směsi? Mr(KCl) = 74,551; Mr(KBr) = 119,00.
Řešení:
Řešení dvousložkového systému je možné na základě navážky směsi
chemických individuí a titrace této směsi. Pro titraci platí, že součet látkových
množství KCl a KBr se rovná látkovému množsví spotřebovaného titrantu:
mKCl + mKBr = 0,200 g = 200 mg
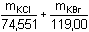 = 18,20 · 0,0996 = 1,81272 mmol
Uvedená soustava dvou rovnic o dvou neznámých umožní zjištění obsahu složek:
| mKCl = 26,355 mg | | wKCl = 13,18 %
| | mKBr = 173,645 mg | | wKBr = 86,82 %
|
Ve směsi draselných halogenidů je 13,18%(m/m) KCl a 86,82%(m/m) KBr.
Zpět
|
|
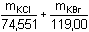 = 18,20 · 0,0996 = 1,81272 mmol
= 18,20 · 0,0996 = 1,81272 mmol