Řešení: Při reakci As2O3 s jodem se AsIII oxiduje na AsV,
čímž nárůstá celkový obsah AsV, a tento nárůst se musí při druhé titraci odečíst.
Stechiometrické poměry složek vyplývají z následujících schémat:
 2 AsIII 2 AsIII
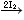 2 AsV + 4 I- 2 AsV + 4 I-
As2O5
 2 AsV 2 AsV
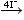 2 AsIII + 2 I2
I2 + 2 S2O32- →
2I- + S4O62- 2 AsIII + 2 I2
I2 + 2 S2O32- →
2I- + S4O62-n(As2O3) = n(I2) · 1/2 = n(As2O5) n(I2) = n(S2O32-) · 1/2 n(As2O5) = n(S2O32-) · 1/4
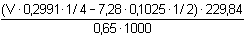
Celková spotřeba 0,2991 molárního thiosíranu bude 23,90 ml. | ||