Řešení: a) Ze vztahu (79) lze vypočítat látkovou koncentraci amonné soli zcela disociované:
[NH4+] = 0,1758 mol·l-1
Při ionizaci chloridu amonného z 81 % je třeba NH4+-iontů úměrně více:
b) Do vztahu (79) lze dosadit přímo určovanou hmotnost NH4Cl:
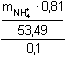
 m(NH4Cl) =
11,61 g·l-1 m(NH4Cl) =
11,61 g·l-1
K přípravě 1 litru amoniakálního pufru o pH 9 je třeba 11,61 g NH4Cl. | ||