Řešení: Objem roztoku po přídavku hydroxidu: V = V1 + V1(0,20/2) = 1,1·V1 Celková koncentrace kyseliny octové:
Koncentrace hydroxoniových iontů (z disociační konstanty):
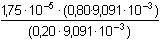 =
7,0·10–5 mol·l-1 =
7,0·10–5 mol·l-1
Vypočtená hodnota [H3O+] je poměrně nízká a je tedy možno použít vztahu pro přibližný výpočet (83) nebo (84):
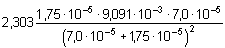 = 0,00335 = 0,00335
Podle (84):
[Ac-] = 0,20 · 9,091·10–3 = 1,818·10–3
mol·l-1
β = 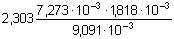 = 0,00335 ≈
0,0034 = 0,00335 ≈
0,0034
Tlumivá kapacita roztoku je 0,0034 (podle vztahu (81) je β = 0,00369). | ||