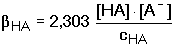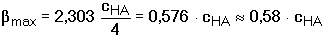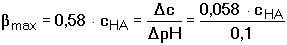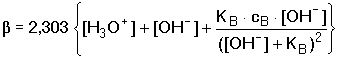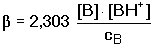| |||||
|
5.7. Kapacita tlumivých roztoků Účinnost pufrů je charakterizována hodnotou tlumivé kapacity (pufračního kvocientu). Je definována poměrem přídavku jednosytné silné zásady B, resp. jednosytné silné kyseliny HA k příslušné změně pH pufru (čím většího látkového množství hydroxidu, resp. kyseliny, přidaného do 1 litru pufru, je třeba pro určité zvýšení, resp. snížení pH, tím lepší je pufr): Při odvozování vztahu tlumivé kapacity kyselého pufru (od slabé kyseliny a konjugované zásady) se vychází z podmínky elektroneutrality [H3O+] + [B+] = [OH-] + [A-] Je-li [B+] = cB a cHA = [HA] + [A-], obdrží se po dosazení disociační konstanty za [A-]
Diferenciací vztahu podle [H3O+] se získá rovnice
Protože platí: V této obecné rovnici jsou zahrnuty i tlumivé kapacity silných elektrolytů (silné kyseliny a silné zásady):
Pro přibližný výpočet tlumivé kapacity pufrů, vytvořených od slabých kyselin HA, obvykle postačuje poslední člen rovnice (81) nebo vztah odvozený z rovnovážných koncentrací konjugovaného páru:
Diferenciací podle cB: Jak výše uvedeno: dosazením dpH za d[H3O+] a úpravou se obdrží
Protože cB = [A-] a Je-li [H3O+] = KHA, pak [HA] = [A-] = cHA/2 a tlumivá kapacita dosahuje maximální hodnoty. Vztah pro βmax lze odvodit z rovnic (82) nebo (83) Z (84) tedy vyplývá, že např. přídavek látkového množství 0,058cHA molu silné zásady nebo silné kyseliny do 1 litru pufru změní pH o 0,1 jednotky pH, neboť platí:
Vzhledem k poklesu aktivitních koeficientů při zvyšování látkové koncentrace elektrolytů lze prakticky dosáhnout nejvyšší hodnoty βmax ≈ 0,2. Analogické vztahy lze odvodit pro tlumivou kapacitu směsí slabých zásad a konjugovaných kyselin: Řešené příklady:
| ||
| |||||

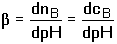
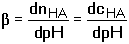 (80)
(80)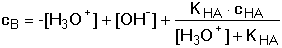
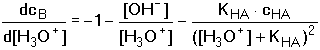
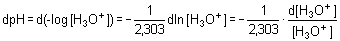 lze dosazením do předchozí rovnice
a úpravou odvodit vztah
lze dosazením do předchozí rovnice
a úpravou odvodit vztah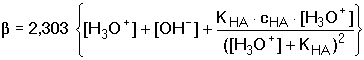
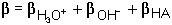
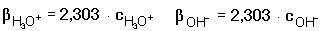
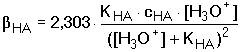
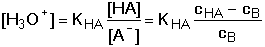
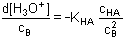
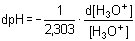
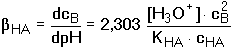
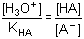 ,
lze snadno odvodit vztah
,
lze snadno odvodit vztah