|
- Příklad 5.61
- Jaká je hodnota pH 0,2 molárního roztoku hydroxidu amonného, který je disociován na 0,955 %?
Řešení:
Disociační stupeň α = 0,00955
a)
[OH-] = cB · α = 0,2 · 0,00955 =
1,91·10–3 mol·l-1
pOH = 2,72 pH = 11,28
Podle
(39)
pH = 14 + log (0,2 · 0,00955) = 11,28
b)
KB = 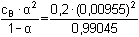 = 1,842·10–5 =
10–4,735 = 1,842·10–5 =
10–4,735
Podle
(36)
pH = 14 – 1/2(4,74 – log 0,2) = 11,28
Protože je splněna podmínka správnosti a), výsledek není třeba upřesňovat. Roztok má pH 11,28.
Zpět
|
|
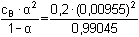 = 1,842·10–5 =
10–4,735
= 1,842·10–5 =
10–4,735