Řešení: Pro vznik sraženiny BaCO3 je v roztoku k disposici látková koncentrace iontů Ba2+ určená součinem rozpustnosti síranu barnatého:
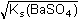 = =
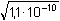 = 1,05·10-5 mol·l-1 = 1,05·10-5 mol·l-1
Pro rovnovážnou koncentraci uhličitanového iontu bude ze součinu rozpustnosti platit
[CO32-] = 4,90·10-4 mol·l-1
[CO32-] = [Na2CO3] =
4,90·10-4 mol·l-1
Ke vzniku sraženiny BaCO3 dojde při koncentraci uhličitanu sodného větší než 4,90·10-4 mol·l-1. | ||