- Příklad VI.2.28




- Roztok dichromanu byl titrován coulometricky v prostředí směsi H2SO4 a
H3PO4 za přítomnosti síranu železito-amonného. Elektrolýza Fe3+-iontů
byla uskutečněna proudem 20 mA a ukončena v bodě ekvivalence za 241,2 s (průběh chemické reakce byl
sledován potenciometricky). Jaké množství (mg) chromu je ve vzorku dichromanu? Mr(Cr) = 52,00
ŘešeníPrůběh chemické reakce: Cr2O72- + 6 Fe2+ + 14 H+ 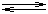 2 Cr3+ + 6 Fe3+ + 7 H2O 2 Cr3+ + 6 Fe3+ + 7 H2O Poměr látkových množství Cr3+ a Fe2+: nCr3+ : nFe2+ = 2 : 6  nCr3+ = nFe2+ · 1/3 nCr3+ = nFe2+ · 1/3 Množství chromu ve vzorku (podle vztahu VI.9): mCr = nCr · MCr = 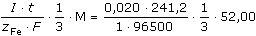 mCr = 8,661·10-4 g = 0,8661 mg Zpět
| 


