- Příklad VI.2.32




- Ionty Mg2+ byly vysráženy při pH 10 jako oxinát Mg(ox)2. Po oddělení byla sraženina
v kyselém prostředí rozpuštěna a uvolněný 8-hydroxychinolin byl titrován bromem vygenerovaným z bromidu
na Pt-anodě. Jaké množství Mg2+–iontů vzorek obsahoval, jestliže při proudu 8 mA trvala analýza
415 vteřin? Mr(Mg) = 24,305. Schéma bromace oxinu (8-hydroxychinolinu):
C9H6N(OH) + 2 Br2 → C9H4N(OH)Br2 + 2 HBr
ŘešeníReakční poměr látkových množství hořčíku, oxinu a bromu: nMg : noxin : nBr2 = 1:2:4; molekula bromu je dvouatomová  celkový počet elektronů v reakci bude 8. celkový počet elektronů v reakci bude 8. Množství Mg2+ ve vzorku (VI.9): mMg = 0,008 · 415 ·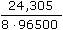 = 1,045·10-4 g = 0,1045 mg = 1,045·10-4 g = 0,1045 mg resp. nBr2 = 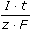 = = 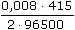 = 1,72·10-5 mol Br2 = 1,72·10-5 mol Br2 nMg = nBr2 · ¼ = 1,72·10-5 · ¼ = 4,30·10-6 mol mMg = nMg · MMg = 1,045·10-4 g = 0,1045 mg Zpět
| 



 celkový počet elektronů v reakci bude 8.
celkový počet elektronů v reakci bude 8.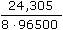 = 1,045·10-4 g =
= 1,045·10-4 g = 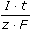 =
= 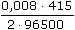 = 1,72·10-5 mol Br2
= 1,72·10-5 mol Br2