|
- Příklad VI.2.35




- Sulfidový anion S2– lze stanovit jako Ag2S stříbrnými ionty generovanými anodickou
oxidací stříbrné elektrody. a) Jakou hodnotu generačního proudu je třeba nastavit, aby při obsahu
1,6 mg S2– byl konec titrace za 200 vteřin? b) Při jakém napětí Ue
je dosaženo bodu ekvivalence (článek tvoří stříbrná a merkurosulfátová elektroda)?
Mr(S) = 32,06; Mr(Ag) = 107,87; Eref = 0,682 V,
Ks(Ag2S) = 1,32·10–50
Řešenía) I = 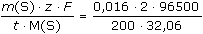 = 0,04816 A = 48,16 mA = 0,04816 A = 48,16 mA nebo 2 n(Ag+) ..... n(S2–)  2 · 107,87 mg Ag+ je ekvivalentní ..... 32,06 mg S2- 2 · 107,87 mg Ag+ je ekvivalentní ..... 32,06 mg S2- m mg Ag+ .............................. 1,6 mg S2-
m(Ag+) = 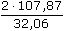 · 1,6 = 10,767 mg · 1,6 = 10,767 mg I = 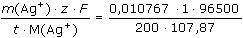 = 0,04816 A = 48,16 mA = 0,04816 A = 48,16 mA b) EAg = EoAg+/Ag + 0,0592 log aAg+ Ks = [Ag+]2[S2-] = 4 [Ag2S]3 [Ag+] = 2 [Ag2S] = 2 · 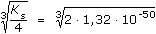 = 3·10–17 mol·l–1 = 3·10–17 mol·l–1 EAg = 0,799 + 0,0592 log 3·10–17 = –0,179 V Ue = E+ - E- = 0,682-(-0,179) = 0,861 V Zpět
|
|