| |
| |
- Příklad 2.18



- Vzorek wolframové oceli o hmotnosti 5,00 g byl převeden do roztoku lučavkou
královskou, roztok byl odpařen a dehydratován. Odparek (H2WO4
+ SiO2) měl hmotnost 0,0928 g. Působením kyseliny fluorovodíkové na odparek
se jeho hmotnost o 20% snížila. Jaký je procentový obsah křemíku a wolframu v oceli?
Rada Reakční schéma:| Si, W → H2WO4 + SiO2 (0,0928 g) | { | SiO2 (20%, tj. 0,01856 g)
H2WO4 (80%, tj. 0,07424g) |
K2SO4·Al2(SO4)3·24H2O → 2 Al(OH)3 → Al2O3 plyne úměra:4 moly S ............................ 1 mol Al2O3 Dosazením molárních hmotností se vypočítá hmotnost S:4 · 32,06 g S ...................... 101,96 g Al2O3m g S ...................... 0,141 g Al2O3
ms = 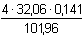 = 0,1773 g S = 0,1773 g Sw s = 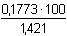 = 12,48 % Obdobnou úměrou se vypočítá hmotnostní obsah K2SO4·Al2(SO4)3·24H2O (Mr = 948,78) ve vzorku a obsah inertních nečistot se získá odečtením procentuality K2SO4·Al2(SO4)3·24H2O od 100 %.Zpět
|
| | |
|
|