Řešení: Označme m1 hmotnost KCl a m2 hmotnost NaCl, pak
Podle vztahu (2)
lze ze známého množství KClO4 vypočítat hmotnost KCl (m1) nebo
přímo K2O:
m1 =
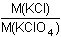 · 0,3330 g = 0,5381 · 0,3330 = 0,1792 g · 0,3330 g = 0,5381 · 0,3330 = 0,1792 gm(K2O) =
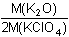 · 0 3330 g = 0,3399 · 0,3330 = 0,1132 g · 0 3330 g = 0,3399 · 0,3330 = 0,1132 gm(K2O) = n(KClO4) ·
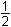 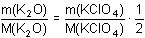 m(K2O) =
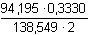 = 0,3399 · 0,3330 = 0,1132 g = 0,3399 · 0,3330 = 0,1132 gOdečtením hmotnosti m1 od celkové hmotnosti směsi chloridů se zjistí hmotnost NaCl m2 = 0,2172 g – 0,1792 g = 0,0380 g NaCl
m(Na2O) =
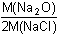 · 0,0380 g = 0,5302 · 0,0380 = 0,0201 g · 0,0380 g = 0,5302 · 0,0380 = 0,0201 gHmotnostní (procentuální) obsah oxidů bude podle (5) w1 =
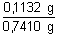 = 0,1528 ...... 15,28% K2O = 0,1528 ...... 15,28% K2Ow2 =
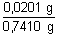 = 0,0271 ...... 2,71% Na2O = 0,0271 ...... 2,71% Na2OVzorek silikátové zeminy obsahuje 15,28%(m/m) K2O a 2,71%(m/m) Na2O. | ||