| |
| |
- Příklad 3.70




- Z roztoku obsahujícího chloridy a bromidy bylo vyizolováno 0,6316 g směsi AgCl a
AgBr. Sraženina byla rozpuštěna v 50 ml 0,1894M-KCN a na přebytečný kyanid se
spotřebovalo 9,81 ml 0,0945M-AgNO3. Jaký je procentový obsah jednotlivých
složek ve směsné sraženině?
Řešení n(KCN)zreag. = 50,00 · 0,1894 – 9,81 · 0,0945 · 2 = 7,6159 mmol = 7,6159·10-3 molSoustava dvou rovnic: m(AgCl) + m(AgBr) = 0,6316 g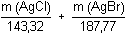 = 37,6159·10 -3 · 1/2 = 3,8080·10 -3 mol Výsledky:m(AgCl) = 0,2690 g  (wAgCl) = 42,59 % (wAgCl) = 42,59 %m(AgBr) = 0,3626 g  (wAgBr) = 57,41 % (wAgBr) = 57,41 % Zpět
|
| | |
|
|