|
- Příklad 3.79
- Vzorek vzduchu objemu 100 ml byl protřepáván s roztokem octanu
kademnatého, pak bylo přidáno 10 ml 0,0552 molárního roztoku jodu a 5 ml 0,1MHCl.
Přebytek jodu byl ztitrován 0,1201M-Na2S2O3 a jeho
spotřeba činila 8,12 ml. Jaká je hmotnost a objemová procentualita H2S
v 1 m3 vzduchu? Mr(H2S) = 34,08.
Řešení:
m(H2S) = (10 · 0,0552 - 8,12 · 0,1201 · 1/2) · 1 ·
34,08 · 10000 = 21945,5 mg = 21,946 g
φ(H 2S) = 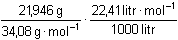
= 0,01443 ..... 1,44 %
V objemu 1 m3 vzduchu bylo 22,946 g, tj. 1,44 % (v/v) H2S.
Zpět
|
|
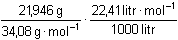 = 0,01443 ..... 1,44 %
= 0,01443 ..... 1,44 %