Řešení: Podle (31b): pH = 1/2(3,68 – log 0,001) = 3,34 Ověřením správnosti zjistíme, že pH < 1,30 – log 0,001 = 4,30 a je tedy nezbytné správnou hodnotu pH vypočítat podle (30) nebo aproximací podle (29).a) Podle (30):
[H3O+] =
pH = 3,44
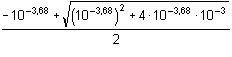 =
3,644·10–4 mol·l-1 =
3,644·10–4 mol·l-1a) Podle (29):
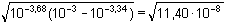 =
3,34·10–4 mol·l-1 =
3,34·10–4 mol·l-1
pH1 = 3,48
Druhá aproximace (s hodnotou pH1 pod odmocninou) a třetí aproximace (s hodnotou pH2 pod odmocninou) poskytnou výsledky: pH2 = 3,43 a pH3 = 3,44. Tyto hodnoty se od sebe liší již nepatrně, proto hodnota pH3 je konečná.
|
| |