Řešení: Ks = [Mg2+][OH–]2 = 4c3 V nasyceném roztoku Mg(OH)2 je podle (7)
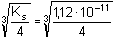 =
1,41·10-4 mol·l-1 =
1,41·10-4 mol·l-1
[OH–] = 2c = 2,82·10-4 mol·l-1
Při koncentraci OH–-iontů 12krát větší, tj. [OH–] =
3,384·10-3 mol·l-1, koncentrace Mg2+-iontů bude
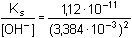 =
9,78·10-7 mol·l-1 =
9,78·10-7 mol·l-1
Koncentrace hořečnatých iontů se zmenší asi 144krát. | ||