|
- Příklad 7.68
- Vypočtěte termodynamickou hodnotu součinu rozpustnosti chloridu stříbrného, jestliže ve směsi
10 ml 0,1M-AgNO3 a 90 ml 0,1M-KCl bylo naměřeno EMN = 0,060 V systémem elektrod Ag – SCE.
EoAg+/Ag = 0,799 V, ESCE = 0,241 V při 25°C.
Řešení:
Podle
(20)
má potenciál stříbrné elektrody hodnotu
EAg = 0,060 + 0,241 = 0,301 V
Podle
(21)
EAg = 0,799 + 0,059 log aAg+ = 0,301 V
log aAg+ = –8,44 = Ks,c / [Cl–]
Koncentrace chloridových iontů v roztoku:
[Cl–] = 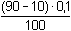 = 8·10–2
mol·l–1 = 10–1,097 mol·l–1 = 8·10–2
mol·l–1 = 10–1,097 mol·l–1
Součin rozpustnosti Ks,c pak bude
Ks,c = 10–8,44 · 10–1,097 ≈ 10–9,54
Termodynamická hodnota součinu rozpustnosti pro I = 0,1 podle vztahu
(5)
pKs,T = 9,54 + 0,24 = 9,78
Hodnota součinu rozpustnosti je Ks,T = 10–9,78 = 1,66·10–10.
Zpět
|
|
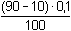 = 8·10–2
mol·l–1 = 10–1,097 mol·l–1
= 8·10–2
mol·l–1 = 10–1,097 mol·l–1