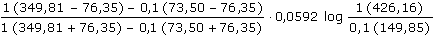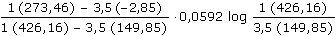|
- Příklad IV.2.5




- Při měření pH roztoku kyseliny chlorovodíkové o koncentraci a) 1 mol·l-1
a b) 10-5 mol·l-1 skleněnou elektrodou byla použita kalomelová referentní
elektroda c) 0,1 molární a d) 3,5 molární (při 25 °C). Kolik milivoltů má v jednotlivých případech
difúzní potenciál a jakou změnu pH tento potenciál představuje za předpokladu, že teoretická směrnice
je 59,2 mV/pH?
ŘešeníMolární iontové vodivosti (tab.2): λoH+ = 349,81; λoK+ = 73,50; λoCl- = 76,35 [S·cm2·mol-1] Komb. ac): EL = 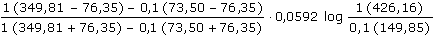 EL = 0,0573 V = 57,3 mV ΔpH = 57,3/59,2 = 0,97 Komb. ad): EL = 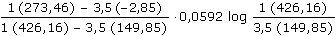 EL = 0,01538 V = 15,4 mV ΔpH = 15,4/59,2 = 0,26 Komb. bc): EL = 0,00403 V = 4,03 mV ΔpH = 4,03/59,2 = 0,07 Komb. bd): EL = 5,73·10-3 V = 5,73 mV ΔpH = 5,73/59,2 = 0,098 ≈ 0,10 Zpět
|
|