|
- Příklad VIII.2.3




- Vzorek směsi kyseliny octové a chlorovodíkové byl v 50 ml odměrné baňce doplněn redestilovanou vodou
po značku. Alikvotní objem 10 ml byl odebrán do kádinky a k němu bylo přidáno 90 ml redestilované vody.
Vzorek byl titrován odměrným roztokem 0,5023 M-NaOH s konduktometrickou indikací bodu ekvivalence.
V průběhu titrace byly zaznamenány následující hodnoty vodivosti G:
| V (ml) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10
| | G (mS) | 6,039 | 4,512 | 3,016 | 1,633 | 1,874 | 2,111 | 2,344 | 2,850 | 3,815 | 4,761 | 5,692
|
Sestrojte titrační křivku z hodnot korigované vodivosti 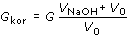 , kde
V0 je počáteční objem titrovaného roztoku a VNaOH objem
přidaného titračního činidla, a určete hmotnostní koncentrace jednotlivých kyselin v původním objemu
50 ml vzorku. Mr(HC1) = 36,465; Mr(CH3COOH) = 60,054. , kde
V0 je počáteční objem titrovaného roztoku a VNaOH objem
přidaného titračního činidla, a určete hmotnostní koncentrace jednotlivých kyselin v původním objemu
50 ml vzorku. Mr(HC1) = 36,465; Mr(CH3COOH) = 60,054.
ŘešeníVýpočet hodnot Gkor: | V (ml) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | | G (mS) | 6,039 | 4,512 | 3,016 | 1,633 | 1,874 | 2,111 | 2,344 | 2,850 | 3,815 | 4,761 | 5,692 | | Gkor (mS) | 6,039 | 4,557 | 3,076 | 1,682 | 1,949 | 2,217 | 2,485 | 3,049 | 4,120 | 5,190 | 6,261 |
Grafické znázornění titrační křivky: 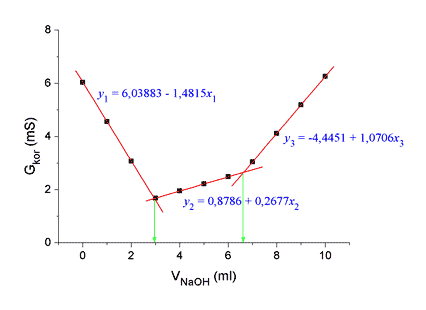
Určení bodů ekvivalence z průsečíků rovnic regresních přímek: 1. bod ekvivalence (spotřeba činidla na reakci HCl + NaOH → NaCl + H2O): 6,03883 – 1,4815x = 0,8786 + 0,2677x x = V1 = 2,95 ml 2. bod ekvivalence: 0,8786 + 0,2677x = -4,4451 + 1,0706x x = Vcelk = 6,63 ml Spotřeba činidla na reakci CH3COOH + NaOH → CH3COONa + H2O: V2 = Vcelk - V1 = 6,63 - 2,95 = 3,68 ml Výpočet obsahu kyselin v 50 ml vzorku: m(HCl) = V1 · cNaOH · M(HCl) · 50/10 = 2,95 ml · 0,5023 mmol/ml · 36,465 mg/mmol · 5 m(HCl) = 270 mg v 50 ml vzorku m(CH3COOH) = V2 · cNaOH · M(CH3COOH) · 50/10 m(CH3COOH) = 3,68 ml · 0,5023 mmol/ml · 60,054 mg/mmol · 5 m(CH3COOH) = 555 mg v 50 ml vzorku Zpět
|
|