|
- Příklad 2.7




- Vzorek thiosíranu sodného byl zoxidován na síran a ten byl srážen chloridem
barnatým jako BaSO4. Z navážky 0,2508g bylo získáno 0,4700g BaSO4.
Jaká je hmotnostní procentualita thiosíranu sodného pentahydrátu ve vzorku?
Řešení Z reakčního schématuNa2S2O3 → 2 Na2SO4 → 2 BaSO4 vyplývá, že z 1 molu Na2S2O3·5H2O se získají 2 moly BaSO4Odtud pro hmotnosti plyne úměra: 248,17 g Na2S2O3·5H2O ..............2 · 233,40 g BaSO4m g Na2S2O3·5H2O ........................0,4700 g BaSO4
m = 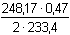 = 0,2499 g Na2S2O3·5H2O = 0,2499 g Na2S2O3·5H2O Hmotnostní procentualita Na2S2O3·5H2O podle (5) budew%(Na2S2O3·5H2O) = 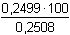 = 99,63 = 99,63 Hmotnostní procentualita thiosíranu sodného pentahydrátu ve vzorku činí 99,63%.Zpět
|
|




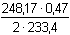 = 0,2499 g Na2S2O3·5H2O
= 0,2499 g Na2S2O3·5H2O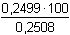 = 99,63
= 99,63