|
- Příklad 3.59




- Ve vzorku o hmotnosti 0,1120 g byl stanoven zinek a hořčík titrací 0,02128
molárním roztokem chelatonu 3. Při titraci na eriochromčerň T v alkalickém
prostředí činila spotřeba 23,81 ml. Další navážka 0,0987 g vzorku byla po rozpuštění
titrována při pH = 5 na xylenolovou oranž (stanovení Zn2+), spotřeba EDTA byla
9,56 ml. Jaký je procentový obsah Zn a Mg ve vzorku?
Řešení Podle (3): (wZn) = 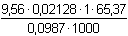 · 100 = 13,47 % · 100 = 13,47 %Spotřeba EDTA na Zn2+ v alkalickém prostředí při navážce vzorku 0,1120 g: V(EDTA)Zn = 9,56 ml · 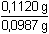 = 10,85 ml = 10,85 ml Podle (3): (wMg) = 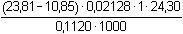 · 100 = 5,98 % · 100 = 5,98 %Zpět
|
|




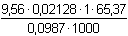 · 100 = 13,47 %
· 100 = 13,47 %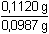 = 10,85 ml
= 10,85 ml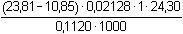 · 100 = 5,98 %
· 100 = 5,98 %