|
- Příklad 3.82
- Na vzorek šťavelanu sodného, znečištěného kyselinou šťavelovou a
inertními nečistotami, hmotnosti 0,2500 g bylo spotřebováno 31,30 ml
0,0234M-KMnO4. Na novou navážku, tentokrát 5,00 g, byla provedena neutralizační
titrace a spotřebovalo se 12,96 ml 0,0498M-NaOH. Jaký je hmotnostní obsah
jednotlivých složek, včetně inertních nečistot, ve směsi?
Mr(Na2C2O4) = 134,00;
Mr(H2C2O4·2H2O) = 126,07.
Řešení:
Z acidobazické titrace se stanoví obsah kyseliny šťavelové (oxalové):
woxal. = 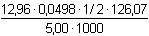 = 0,0081 ..... 0,81 %
= 0,0081 ..... 0,81 %
Pro zjištění obsahu šťavelanu sodného ve vzorku je nutno od celkové spotřeby
manganistanu odečítat spotřebu titrantu na kyselinu šťavelovou.
Procentový obsah 0,81% kyseliny šťavelové v navážce 0,2500 g představuje
hmotnost 0,002025 g. Na toto množství kyseliny se manganistanu spotřebuje
(rovnice viz příklad 3.72.) podle
(1)
a (4)
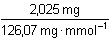 = V · 0,0234 mmol·ml-1 · 5/2 = V · 0,0234 mmol·ml-1 · 5/2
V = 0,275 ml 0,0234M-KMnO4
Obsah šťavelanu pak podle
(3)
bude
wNaOx = 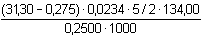 = 0,9728 ..... 97,28 %
= 0,9728 ..... 97,28 %
Obsah inertních nečistot: 100 – (97,28 + 0,81) = 1,91 %
Vzorek obsahoval 97,28%(m/m) Na2C2O4,
0,81%(m/m) H2C2O4·2H2O a
1,91%(m/m) inertních nečistot.
Zpět
|
|
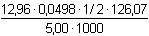 = 0,0081 ..... 0,81 %
= 0,0081 ..... 0,81 %
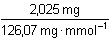 = V · 0,0234 mmol·ml-1 · 5/2
= V · 0,0234 mmol·ml-1 · 5/2
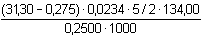 = 0,9728 ..... 97,28 %
= 0,9728 ..... 97,28 %