|
3.1. Neutralizační titrace
3.1.1. Koncentrace odměrných roztoků
Odměrné roztoky přesné koncentrace se připravují z tzv. volumetrických standardů.
Pokud však nemáme látky v definovaném stavu (většina kyselin, hydroxidů), můžeme
připravit jejich roztoky pouze s přibližnou koncentrací. Jejich přesnou látkovou
koncentraci (titr) zjistíme tak, že je "stavíme" na přesné roztoky nebo odvážená množství
standardů.
Pro stanovení titru pak může posloužit rovnice
(1)
upravená podle definičního vztahu látkového množství
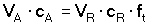 (4) (4)
Řešené příklady:
- Příklad 3.1

- Jakou látkovou koncentraci má roztok hydroxidu sodného, jestliže bylo spotřebováno
a) 9,88 ml roztoku NaOH na 10 ml 0,05M-H2C2O4?
b) 9,68 ml 0,1000M-H2C2O4 na 10 ml NaOH ?
c) 10,05 ml NaOH na 10 ml 0,0989M-HCl ?
- Příklad 3.2

- Jaká je látková koncentrace roztoku kyseliny sírové, jestliže při titraci
navážky 31,87 mg standardu KHCO3 bylo spotřebováno 6,52 ml kyseliny?
Mr(KHCO3) = 100,12.
- Příklad 3.3

- Jakou hmotnost by měla mít navážka trihydrogenoxalátu draselného
(KHC2O4·H2C2O4·2H2O)
pro stanovení titru hydroxidu sodného, jestliže spotřeba přibližně 0,1M-NaOH by měla činit
9,0 ml? Mr(oxalát) = 254,19.
|
|