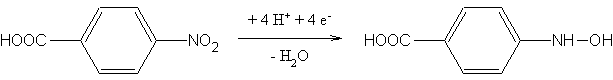|
- Příklad VI.1.10




- Na rtuťové katodě při potenciálu –1,50 V (vs. SKE) byla ve ftalátovém tlumiči (pH 2,65) redukována
kyselina p-nitrobenzoová. Elektrolýza 0,112 ml 1,10·10–3 molárního roztoku analytu
probíhala 125 minut. Na počátku byl proud 10,59 μA, na konci 2,07 μA. Kolik elektronů se zúčastňuje
elektrodové reakce? Mr = 167,124
ŘešeníVýpočet prošlého náboje – rov. (VI.4), (VI.5): log 2,07 μA = log 10,59 μA – k · 7500 k = 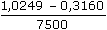 = 9,452·10–5 s–1 = 9,452·10–5 s–1 Q = 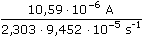 = 0,0486 C (A·s) = 0,0486 C (A·s) Počet elektronů zapojených do elektrodové reakce (VI.1): m = c·V·M = 1,10·10–3 · (0,112·10–3) · 167,124 = 2,059·10–5 g z = Q 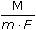 = 0,0486 = 0,0486 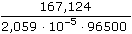 = 4,09 el. = 4,09 el. Mechanismus elektrodové reakce: 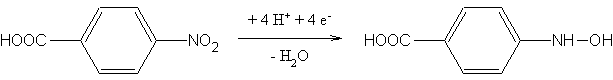
Zpět
|
|




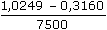 = 9,452·10–5 s–1
= 9,452·10–5 s–1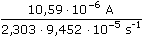 = 0,0486 C (A·s)
= 0,0486 C (A·s)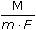 = 0,0486
= 0,0486 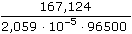 =
=