|
- Příklad VI.1.7




- Roztok 100 ml 0,001M-CdSO4, obsahující 0,1M-KNO3 jako základní elektrolyt, byl
elektrolyzován na rtuťové velkoplošné katodě (10 cm2) při konstantním potenciálu –0,90 V
(vs. SKE), roztok byl míchán konstantní rychlostí. Počáteční proud Io byl 27,02 mA,
koeficient k = 0,0365 min–1
a) Jaký byl proud v časech 1, 5, 10, 15, 30, 60 min?
b) Za jakou dobu klesne koncentrace Cd2+-iontů na tisícinu původní hodnoty?
Řešenía) Proud v jednotlivých časech (rov. VI.5): log It = log Io – k t = log 27,02 – 0,0365·t = 1,4317 – 0,0365·t Výsledky: It [mA] = 24,84 (1 min); 17,75 (5min); 11,66 (10 min); 7,66 (15 min); 2,17 (30 min); 0,17 (60min). b) Proud při elektrolýze je úměrný koncentraci analytu v roztoku, takže platí (VI.7) 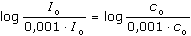 = k t = k t  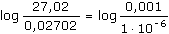 = 0,0365·t = 0,0365·t
t = log 1000 / 0,0365 = 3/0,0365 = 82,19 min = 1h 22min 11s Zpět
|
|




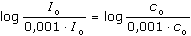 = k t
= k t 
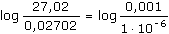 = 0,0365·t
= 0,0365·t