|
- Příklad VI.1.9




- Na Hg-elektrodě bylo při potenciálu –1,80 V (SKE) redukováno 100 ml 2,15·10–3 molárního
roztoku SeO32- při pH 8,9. Jaký je náboj spotřebovaný při elektrolýze a počet
elektronů? Z naměřených hodnot sestrojte grafické závislosti.
| t | 72 | 180 | 360 | 720 | 1080 | 1440 | 1800 | 2520 | 3600 s
| | It | 157 | 135 | 105 | 63,7 | 39,5 | 23,4 | 14,2 | 5,23 | 1,17 mA
| | log It | 2,190 | 2,130 | 2,021 | 1,804 | 1,597 | 1,369 | 1,152 | 0,719 | 0,068
|
ŘešeníSoustava dvou rovnic (rov. VI.5) pro výpočet k a Io: log 157 = log Io – k · 72 log 1,17 = log Io – k · 3600 |·(-1)
log 157 - log 1,17 = (3600-72)k k = 6,032·10–4 s–1; log Io = 2,239  Io = 173,38 mA = 0,1738 A Io = 173,38 mA = 0,1738 A Náboj (VI.4): Q = 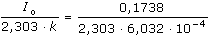 = 125,11 C = 125,11 C Elektrony: n = 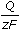 = c V = c V  z = z = 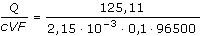 = 6,03 el. = 6,03 el. Elektrodová reakce: SeO32- + 8 H+ + 6 e– → H2Se + 3 H2O 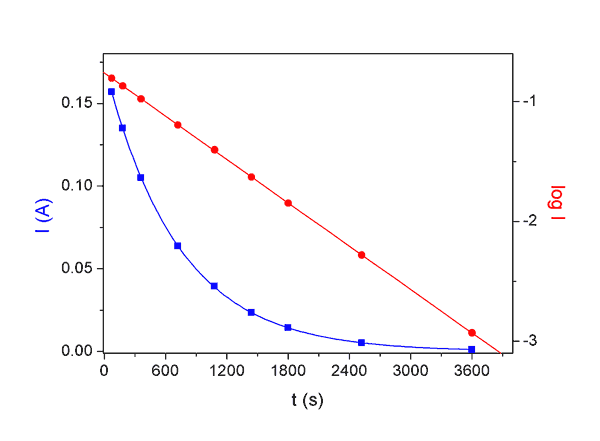
Grafické závislosti proudu a logaritmu proudu na čase
pro coulometrickou redukci 2,15·10–3 M-SeO32- na Hg-elektrodě při pH 8,9.Zpět
|
|




 Io = 173,38 mA = 0,1738 A
Io = 173,38 mA = 0,1738 A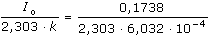 =
= 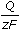 = c V
= c V 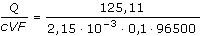 =
= 