| |
| |
- Příklad 3.37




- Vzorek olea hmotnosti 1,500 g spotřeboval při titraci na fenolftalein 21,64 ml
1,50M-KOH. Jaký je hmotnostní obsah volného SO3 a H2SO4,
jestliže oleum kromě SO3 a H2SO4 obsahuje také
2,06 %(m/m) SO2?
Řešení Kyselé složky ve vzorku olea jsou H2SO4, volný SO3 a SO2 (2,06 % m/m).m(SO 2) = 0,0206 · 1,500 = 0,0309 g  n(SO 2) = 4,8236·10 -4 mol VKOH · 1,50 mmol·ml–1 = 0,48236 mmol · 2VKOH = 0,6432 ml 1,50 molárního roztoku Celkový obsah SO3 (podle vztahů (2) a (3)):m(SO3)celk. = (21,64 – 0,6432) · 1,50 · 1/2 · 80,06 = 1260,7528 mg = 1,2608 gw(SO3)celk. = 1,2608 g / 1,500 g = 0,8405, tj. 84,05 % Množství vody sloučené s SO3: mvz. – m(SO2) – m(SO3)celk.m(H2O) = 1,500 g – (0,0309 + 1,2608) g = 0,2083 g Množství vázaného SO3: n(SO3) = n(H2O)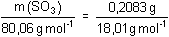  m(SO3)váz. = 0,9260 g m(SO3)váz. = 0,9260 g
Hmotnostní obsah volného SO3:m(SO3)celk. – m(SO3)váz = 0,3348 g v 1,5 g oleaw(SO3)vol. = 0,2232, tj. 22,32 % Hmotnostní obsah H2SO4: n(H2SO4) = n(H2O)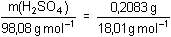  m(H2SO4) = 1,1344 g v 1,5 g olea m(H2SO4) = 1,1344 g v 1,5 g oleaw(H2SO4) = 0,7562, tj. 75,62 %
Zpět
|
| | |
|
|




 n(SO2) = 4,8236·10-4 mol
n(SO2) = 4,8236·10-4 mol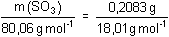
 m(SO3)váz. = 0,9260 g
m(SO3)váz. = 0,9260 g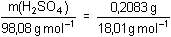
 m(H2SO4) = 1,1344 g v 1,5 g olea
m(H2SO4) = 1,1344 g v 1,5 g olea