| |
| |
- Příklad 3.92




- Zlato bylo stanoveno nepřímou metodou v prostředí difosforečnanu retitrací
manganaté soli manganistanem:
Au3+ + 3 Mn2+ + 9 H2P2O72-
→
Au + 3 [Mn(H2P2O7)3]3-
4 Mn2+ + MnO4- + 15 H2P2O72-
+ 8 H+  5 [Mn(H2P2O7)3]3- + 4 H2O
5 [Mn(H2P2O7)3]3- + 4 H2O
Roztok zlatité soli byl připraven rozpuštěním 1,0150 g AuCl3·2H2O
ve zředěné HCl a objem byl upraven na 250 ml. Podíl 10,00 ml byl přelit 20,00 ml roztoku
MnSO4 (10 ml odpovídá 2,25 ml 0,05814M-KMnO4) a na retitraci bylo
spotřebováno 2,96 ml 0,05814M-KMnO4. Jaký je hmotnostní obsah zlata ve vzorku
a jaká je látková koncentrace zlatité soli?
Řešení Látková koncentrace roztoku MnSO4 (podle rovnice (4)):10 ml · c = 2,25 ml · 0,05814 mmol/ml · 4c(MnSO 4) = 0,05233 mmol·ml –1 = mol·l –1Hmotnostní obsah zlata v roztoku objemu 250 ml, řešení podle (3): w(Au) = 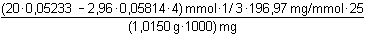 · 100 = 57,93 % · 100 = 57,93 % Látková koncentrace roztoku 250 ml zlatité soli (řešení vyplývá z čitatele zlomku w(Au)) nebo podle rovnice (2)): m(Au) = (20 · 0,05233 - 2,96 · 0,05814 ·4) · 1/3 ·196,97 · 25 = 587,99 mgc(AuCl 3) = 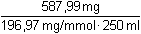 = 0,01194 mmol·ml–1 = mol·l –1 Zpět
| | |
| |
|




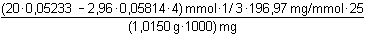 · 100 = 57,93 %
· 100 = 57,93 %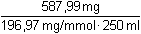 = 0,01194 mmol·ml–1 = mol·l–1
= 0,01194 mmol·ml–1 = mol·l–1