



Řešení Vlivem přídavku silného hydroxidu vznikne ekvivalentní množství octanu (konjugované báze); současně se zvětší objem celková koncentrace kyseliny klesne. celková koncentrace kyseliny klesne.a)
Celková koncentrace kyseliny: cHac = 0,01 / 1,05 = 9,524·10-3 mol·l-1
 KHac = 1,754·10-5 KHac = 1,754·10-5
 [H+] = 5,262·10-5 mol·l-1 [H+] = 5,262·10-5 mol·l-1resp. [H+] = 1,754·10-5 · (75/25) = 5,262·10-5 mol·l-1
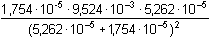 = 4,11·10-3 = 4,11·10-3
[Ac–] = 0,25 · 0,01 / 1,05 = 2,381·10-3 mol·l-1 β = 2,303 · 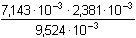 = 4,11·10-3 = 4,11·10-3b) Řešení je analogické podle a). | ||