



Řešení K výpočtu rozpustnosti uhličitanu stříbrného ovlivněné iontovou sílou roztoku (vytvořenou ionty Ag+ a CO32–) lze použít několik postupů. Základem je hodnota rozpustnosti sloučeniny zjištěná podle vztahu (7) z termodynamického součinu rozpustnosti. Ks = 8,13·10–12, pKs = 11,09
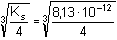 = 1,27·10–4 mol·l-1 = 1,27·10–4 mol·l-1I = 1/2(2·1,27·10–4·12 + 1,27·10–4·22) = 3,81·10–4
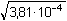 = –0,00994 = –0,00994  fAg+ = 0,977 fAg+ = 0,977log fCO32- = –0,509·22· Ks,c = 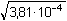 = –0,00397 = –0,00397  fCO32- = 0,912 fCO32- = 0,912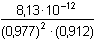 = 9,546·10–12 = 10–11,02 = 9,546·10–12 = 10–11,02[Ag2CO3] = 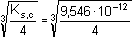 = 1,33·10–4 mol·l-1 = 1,33·10–4 mol·l-1nebo lze využít středního aktivitního koeficientu sloučeniny:
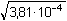 = –0,01987 = –0,01987  f± = 0,955 f± = 0,955Ks,c = [Ag2CO3] = 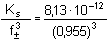 = 9,334·10–12 = 10–11,03 = 9,334·10–12 = 10–11,03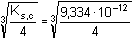 = 1,33·10–4 mol·l-1 = 1,33·10–4 mol·l-1
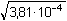 = –3,8763 = –3,8763 [Ag2CO3] = 1,33·10–4 mol·l-1 | ||