|
- Příklad IV.1.10




- Jaký bude rovnovážný potenciál argentochloridové elektrody v roztoku 0,0500M-HCl
(f± = 0,830) vzhledem k vodíkové elektrodě, sycené vodíkem při atmosférickém
tlaku 99,58 kPa, teplotě 25 °C a tensi vodních páry 3,11 kPa.
ŘešeníEoAgCl/Ag = -0,222 V (z tab. 1) Potenciál vodíkové elektrody (IV.3): EH = Eo + 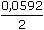 log log  = 0,0 + = 0,0 + 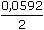 log log 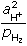 aH+ = 0,05 · 0,830 = 0,0415 mol/l = aCl- pH2 = 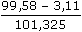 = 0,9521 kPa = 0,9521 kPa EH = 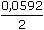 log log 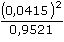 = -0,0812 ≈ -0,081 V = -0,0812 ≈ -0,081 V EAgCl = 0,222 - 0,0592 log aCl- = 0,222 - 0,0592 log 0,0415 ≈ 0,304 V Ue = E+ - E- = Eref - EH = 0,304 - (-0,081) = 0,385 V Zpět
|
|




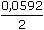 log
log  = 0,0 +
= 0,0 + 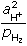
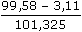 = 0,9521 kPa
= 0,9521 kPa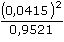 = -0,0812 ≈ -0,081 V
= -0,0812 ≈ -0,081 V